Peptides គឺជាក្រុមនៃសមាសធាតុដែលបង្កើតឡើងដោយការភ្ជាប់នៃអាស៊ីតអាមីណូជាច្រើនតាមរយៈចំណង peptide ។ពួកវាមានគ្រប់ទីកន្លែងនៅក្នុងសារពាង្គកាយមានជីវិត។រហូតមកដល់ពេលនេះ សារធាតុ peptides រាប់ម៉ឺនត្រូវបានគេរកឃើញនៅក្នុងសារពាង្គកាយមានជីវិត។Peptides ដើរតួយ៉ាងសំខាន់ក្នុងការធ្វើនិយតកម្មសកម្មភាពមុខងារនៃប្រព័ន្ធផ្សេងៗ សរីរាង្គ ជាលិកា និងកោសិកា និងក្នុងសកម្មភាពជីវិត ហើយជារឿយៗត្រូវបានគេប្រើក្នុងការវិភាគមុខងារ ការស្រាវជ្រាវអង្គបដិប្រាណ ការអភិវឌ្ឍន៍ថ្នាំ និងវិស័យផ្សេងៗទៀត។ជាមួយនឹងការអភិវឌ្ឍនៃបច្ចេកវិទ្យាជីវសាស្រ្ត និងបច្ចេកវិទ្យាសំយោគ peptide ថ្នាំ peptide កាន់តែច្រើនត្រូវបានបង្កើតឡើង និងអនុវត្តនៅក្នុងគ្លីនិក។
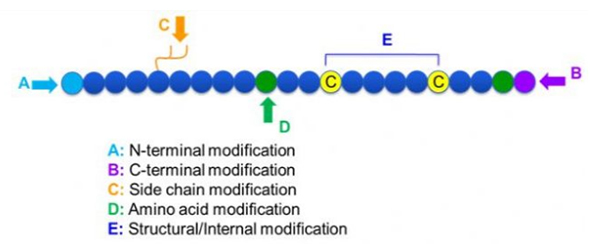
មានការកែប្រែ peptide ជាច្រើនប្រភេទ ដែលអាចបែងចែកយ៉ាងសាមញ្ញទៅជាការកែប្រែក្រោយ និងការកែប្រែដំណើរការ (ដោយប្រើការកែប្រែអាស៊ីតអាមីណូដែលបានមកពី) និងការកែប្រែ N-terminal, C-terminal modification, side chain modification, amino acid modification, skeleton modification, ល អាស្រ័យលើកន្លែងកែប្រែ (រូបភាពទី១)។ជាមធ្យោបាយដ៏សំខាន់មួយដើម្បីផ្លាស់ប្តូររចនាសម្ព័ន្ធខ្សែសង្វាក់មេ ឬក្រុមខ្សែសង្វាក់ចំហៀងនៃសង្វាក់ peptide ការកែប្រែ peptide អាចផ្លាស់ប្តូរលក្ខណៈសម្បត្តិរូបវន្ត និងគីមីនៃសមាសធាតុ peptide ប្រកបដោយប្រសិទ្ធភាព បង្កើនការរលាយទឹក ពន្យារពេលវេលាសកម្មភាពនៅក្នុង vivo ផ្លាស់ប្តូរការចែកចាយជីវសាស្រ្តរបស់ពួកគេ លុបបំបាត់ភាពស៊ាំ។ កាត់បន្ថយផលប៉ះពាល់ពុល។ល។ នៅក្នុងក្រដាសនេះ យុទ្ធសាស្រ្តកែប្រែ peptide សំខាន់ៗមួយចំនួន និងលក្ខណៈរបស់ពួកគេត្រូវបានណែនាំ។
1. Cyclization
Cyclic peptides មានកម្មវិធីជាច្រើននៅក្នុង biomedicine ហើយ peptides ធម្មជាតិជាច្រើនដែលមានសកម្មភាពជីវសាស្រ្តគឺជា cyclic peptides ។ដោយសារ peptides cyclic មាននិន្នាការរឹងជាង peptides លីនេអ៊ែរ ពួកវាមានភាពធន់ទ្រាំខ្លាំងចំពោះប្រព័ន្ធរំលាយអាហារ អាចរស់រានមានជីវិតក្នុងបំពង់រំលាយអាហារ និងបង្ហាញពីភាពស្និទ្ធស្នាលកាន់តែខ្លាំងសម្រាប់អ្នកទទួលគោលដៅ។Cyclization គឺជាវិធីផ្ទាល់បំផុតក្នុងការសំយោគ peptides cyclic ជាពិសេសសម្រាប់ peptides ដែលមានគ្រោងឆ្អឹងធំ។យោងទៅតាមរបៀបវដ្ត វាអាចត្រូវបានបែងចែកទៅជាប្រភេទខ្សែសង្វាក់ចំហៀង ស្ថានីយ - ប្រភេទខ្សែសង្វាក់ចំហៀង ស្ថានីយ - ប្រភេទស្ថានីយ (ប្រភេទចុងដល់ចុង)។
(1) sidechain-to-sidechain
ប្រភេទទូទៅបំផុតនៃខ្សែសង្វាក់ចំហៀងទៅខ្សែសង្វាក់ចំហៀងគឺ disulfide ស្ពានរវាងសំណល់ cysteine ។វដ្តនេះត្រូវបានណែនាំដោយសំណល់ cysteine មួយគូដែលត្រូវបានការពារ ហើយបន្ទាប់មកកត់សុីដើម្បីបង្កើតជាចំណង disulfide ។ការសំយោគ Polycyclic អាចត្រូវបានសម្រេចដោយការដកយកចេញដោយជ្រើសរើសក្រុមការពារ sulfhydryl ។Cyclization អាចត្រូវបានធ្វើទាំងនៅក្នុងសារធាតុរំលាយក្រោយការបែកខ្ញែក ឬនៅលើជ័រដែលមានមុនបំបែក។ការស៊ីក្លូនៅលើជ័រអាចមានប្រសិទ្ធភាពតិចជាងការស៊ីក្លូសូលុយស្យុង ពីព្រោះ peptides នៅលើជ័រមិនងាយបង្កើតទម្រង់ស៊ីក្លូ។ប្រភេទមួយទៀតនៃសង្វាក់ចំហៀង - សង្វាក់ចំហៀងគឺជាការបង្កើតរចនាសម្ព័ន្ធអាមីដរវាងសំណល់អាស៊ីត aspartic ឬអាស៊ីត glutamic និងអាស៊ីតអាមីណូមូលដ្ឋាន ដែលតម្រូវឱ្យក្រុមការពារខ្សែសង្វាក់ចំហៀងត្រូវតែអាចជ្រើសរើសចេញពី polypeptide បាន។ នៅលើជ័រឬបន្ទាប់ពីការបំបែក។ប្រភេទទី 3 នៃសង្វាក់ចំហៀង - សង្វាក់ចំហៀងគឺជាការបង្កើត diphenyl ethers ដោយ tyrosine ឬ p-hydroxyphenylglycine ។ប្រភេទនៃវដ្តនេះនៅក្នុងផលិតផលធម្មជាតិត្រូវបានរកឃើញតែនៅក្នុងផលិតផលអតិសុខុមប្រាណប៉ុណ្ណោះ ហើយផលិតផល cyclization ជាញឹកញាប់មានតម្លៃឱសថសក្តានុពល។ការរៀបចំនៃសមាសធាតុទាំងនេះតម្រូវឱ្យមានលក្ខខណ្ឌប្រតិកម្មតែមួយគត់ដូច្នេះពួកវាមិនត្រូវបានគេប្រើជាញឹកញាប់ក្នុងការសំយោគ peptides សាមញ្ញទេ។
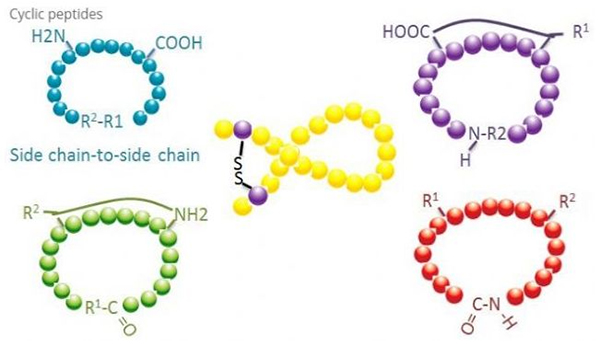
(2) ស្ថានីយ-ទៅ-ខ្សែសង្វាក់
វដ្តសង្វាក់ខាងស្ថានីយជាធម្មតាពាក់ព័ន្ធនឹងស្ថានីយ C ជាមួយក្រុមអាមីណូនៃខ្សែសង្វាក់ចំហៀង lysine ឬ ornithine ឬ N-terminal ជាមួយនឹងខ្សែសង្វាក់ចំហៀងនៃអាស៊ីត aspartic ឬអាស៊ីត glutamic ។វដ្ត polypeptide ផ្សេងទៀតត្រូវបានធ្វើឡើងដោយបង្កើតចំណងអេធើររវាងស្ថានីយ C និងខ្សែសង្វាក់ចំហៀង serine ឬ threonine ។
(3) ប្រភេទស្ថានីយ ឬក្បាលទៅកន្ទុយ
ខ្សែសង្វាក់ polypeptides អាចត្រូវបានបង្វិលនៅក្នុងសារធាតុរំលាយ ឬជួសជុលនៅលើជ័រដោយវដ្តសង្វាក់ចំហៀង។កំហាប់ទាបនៃ peptides គួរតែត្រូវបានប្រើនៅក្នុងការកណ្តាលសារធាតុរំលាយដើម្បីជៀសវាង oligomerization នៃ peptides ។ទិន្នផលនៃ polypeptide ចិញ្ចៀនសំយោគពីក្បាលទៅកន្ទុយគឺអាស្រ័យលើលំដាប់នៃខ្សែសង្វាក់ polypeptide ។ដូច្នេះ មុននឹងរៀបចំ cyclic peptides ក្នុងទ្រង់ទ្រាយធំ បណ្ណាល័យនៃ peptides សំណដែលមានច្រវាក់ដែលអាចធ្វើបានដំបូងគួរតែត្រូវបានបង្កើត ហើយបន្ទាប់មកដោយ cyclization ដើម្បីស្វែងរកលំដាប់ជាមួយនឹងលទ្ធផលល្អបំផុត។
2. N-methylation
N-methylation ដើមឡើយកើតឡើងនៅក្នុង peptides ធម្មជាតិ ហើយត្រូវបានបញ្ចូលទៅក្នុងសំយោគ peptide ដើម្បីការពារការបង្កើតចំណងអ៊ីដ្រូសែន ដោយហេតុនេះធ្វើឱ្យ peptides មានភាពធន់នឹងការបំផ្លិចបំផ្លាញ និងការបោសសំអាតជីវគីមី។ការសំយោគ peptides ដោយប្រើ N-methylated amino acid derivatives គឺជាវិធីសាស្ត្រសំខាន់បំផុត។លើសពីនេះទៀតប្រតិកម្ម Mitsunobu នៃ N-(2-nitrobenzene sulfonyl chloride) polypeptide-resin intermediates ជាមួយមេតាណុលក៏អាចត្រូវបានប្រើផងដែរ។វិធីសាស្រ្តនេះត្រូវបានប្រើដើម្បីរៀបចំបណ្ណាល័យស៊ីលីក peptide ដែលមានអាស៊ីតអាមីណូ N-methylated ។
3. Phosphorylation
Phosphorylation គឺជាផ្នែកមួយនៃការកែប្រែក្រោយការបកប្រែទូទៅបំផុតនៅក្នុងធម្មជាតិ។នៅក្នុងកោសិកាមនុស្សច្រើនជាង 30% នៃប្រូតេអ៊ីនត្រូវបាន phosphorylated ។Phosphorylation ជាពិសេស phosphorylation ដែលអាចបញ្ច្រាស់បាន ដើរតួនាទីយ៉ាងសំខាន់ក្នុងការគ្រប់គ្រងដំណើរការកោសិកាជាច្រើនដូចជា ការបញ្ជូនសញ្ញា ការបញ្ចេញហ្សែន វដ្តកោសិកា និងបទប្បញ្ញត្តិ cytoskeleton និង apoptosis ។
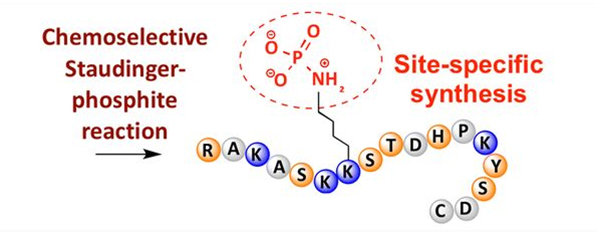
Phosphorylation អាចត្រូវបានគេសង្កេតឃើញនៅភាពខុសគ្នានៃសំណល់អាស៊ីតអាមីណូ ប៉ុន្តែគោលដៅ phosphorylation ទូទៅបំផុតគឺសំណល់ serine, threonine និង tyrosine ។Phosphotyrosine, phosphothreonine, និង phosphoserine derivatives អាចត្រូវបានបញ្ចូលទៅក្នុង peptides កំឡុងពេលសំយោគ ឬបង្កើតឡើងបន្ទាប់ពីការសំយោគ peptide។phosphorylation ជ្រើសរើសអាចត្រូវបានសម្រេចដោយប្រើសំណល់នៃ serine, threonine និង tyrosine ដែលជ្រើសរើសក្រុមការពារ។សារធាតុ phosphorylation មួយចំនួនក៏អាចណែនាំក្រុមអាស៊ីត phosphoric ចូលទៅក្នុង polypeptide ដោយការកែប្រែក្រោយ។ក្នុងប៉ុន្មានឆ្នាំថ្មីៗនេះ phosphorylation ជាក់លាក់នៃគេហទំព័ររបស់ lysine ត្រូវបានសម្រេចដោយប្រើប្រតិកម្ម Staudinger-phosphite ដែលជ្រើសរើសដោយគីមី (រូបភាពទី 3) ។
4. Myristoylation និង palmitoylation
Acylation នៃ N-terminal ជាមួយនឹងអាស៊ីតខ្លាញ់អនុញ្ញាតឱ្យ peptides ឬប្រូតេអ៊ីនភ្ជាប់ទៅនឹងភ្នាសកោសិកា។លំដាប់ myridamoylated នៅលើ N-terminal អនុញ្ញាតឱ្យ kinases ប្រូតេអ៊ីនគ្រួសារ Src និង reverse transcriptase Gaq proteins ត្រូវបានកំណត់គោលដៅដើម្បីចងភ្ជាប់ទៅនឹងភ្នាសកោសិកា។អាស៊ីត Myristic ត្រូវបានភ្ជាប់ទៅនឹង N-terminal នៃជ័រ-polypeptide ដោយប្រើប្រតិកម្មនៃការភ្ជាប់ស្តង់ដារ ហើយ lipopeptide លទ្ធផលអាចត្រូវបានបំបែកនៅក្រោមលក្ខខណ្ឌស្តង់ដារ និងបន្សុតដោយ RP-HPLC ។
5. Glycosylation
Glycopeptides ដូចជា vancomycin និង teicolanin គឺជាថ្នាំអង់ទីប៊ីយោទិចដ៏សំខាន់សម្រាប់ការព្យាបាលការឆ្លងមេរោគបាក់តេរីដែលធន់នឹងថ្នាំ ហើយ glycopeptides ផ្សេងទៀតត្រូវបានគេប្រើជាញឹកញាប់ដើម្បីជំរុញប្រព័ន្ធភាពស៊ាំ។លើសពីនេះទៀត ដោយសារអង់ទីករអតិសុខុមប្រាណជាច្រើនត្រូវបាន glycosylated វាមានសារៈសំខាន់ណាស់ក្នុងការសិក្សា glycopeptides សម្រាប់ការកែលម្អប្រសិទ្ធភាពព្យាបាលនៃការឆ្លងមេរោគ។ម៉្យាងវិញទៀត វាត្រូវបានគេរកឃើញថា ប្រូតេអ៊ីននៅលើភ្នាសកោសិកានៃកោសិកាដុំសាច់បង្ហាញ glycosylation មិនធម្មតាដែលធ្វើឱ្យ glycopeptides ដើរតួនាទីយ៉ាងសំខាន់ក្នុងការស្រាវជ្រាវការពារជំងឺមហារីក និងដុំសាច់។Glycopeptides ត្រូវបានរៀបចំដោយវិធីសាស្ត្រ Fmoc/t-Bu ។សំណល់ glycosylated ដូចជា threonine និង serine ជារឿយៗត្រូវបានបញ្ចូលទៅក្នុង polypeptides ដោយ pentafluorophenol ester បានធ្វើឱ្យសកម្ម fMOCs ដើម្បីការពារអាស៊ីតអាមីណូ glycosylated ។
6. អ៊ីសូព្រីន
Isopentadienylation កើតឡើងនៅលើសំណល់ cysteine នៅក្នុងខ្សែសង្វាក់ចំហៀងនៅជិតស្ថានីយ C ។ប្រូតេអ៊ីន isoprene អាចធ្វើអោយប្រសើរឡើងនូវភាពស្និទ្ធស្នាលនៃភ្នាសកោសិកា និងបង្កើតអន្តរកម្មប្រូតេអ៊ីន-ប្រូតេអ៊ីន។ប្រូតេអ៊ីន Isopentadienated រួមមាន tyrosine phosphatase, GTase តូច, ម៉ូលេគុល cochaperone, nuclear lamina និងប្រូតេអ៊ីនចងកណ្តាល។Isoprene polypeptides អាចត្រូវបានរៀបចំដោយប្រើ isoprene នៅលើជ័រ ឬដោយការណែនាំអំពីនិស្សន្ទវត្ថុ cysteine ។
7. ការកែប្រែ Polyethylene glycol (PEG)
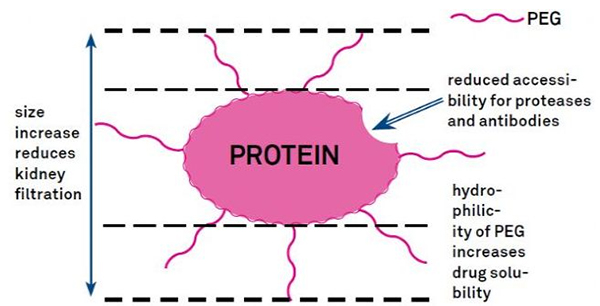
ការកែប្រែ PEG អាចត្រូវបានប្រើដើម្បីធ្វើអោយប្រសើរឡើងនូវស្ថេរភាពអ៊ីដ្រូលីកប្រូតេអ៊ីន ការចែកចាយជីវសាស្រ្ត និងការរលាយ peptide ។ការណែនាំនៃខ្សែសង្វាក់ PEG ទៅនឹង peptides អាចធ្វើអោយប្រសើរឡើងនូវលក្ខណៈសម្បត្តិឱសថសាស្ត្ររបស់ពួកគេហើយក៏រារាំង hydrolysis នៃ peptides ដោយអង់ស៊ីម proteolytic ផងដែរ។PEG peptides ឆ្លងកាត់ផ្នែកឆ្លងកាត់ glomerular capillary យ៉ាងងាយស្រួលជាង peptides ធម្មតា ដោយកាត់បន្ថយការបោសសំអាតតម្រងនោមយ៉ាងខ្លាំង។ដោយសារអាយុកាលពាក់កណ្តាលសកម្មនៃ PEG peptides នៅក្នុង vivo កម្រិតនៃការព្យាបាលធម្មតាអាចត្រូវបានរក្សាជាមួយនឹងកម្រិតទាប និងថ្នាំ peptide មិនសូវញឹកញាប់។ទោះជាយ៉ាងណាក៏ដោយការកែប្រែ PEG ក៏មានឥទ្ធិពលអវិជ្ជមានផងដែរ។បរិមាណដ៏ច្រើននៃ PEG រារាំងអង់ស៊ីមពីការបំផ្លិចបំផ្លាញ peptide និងកាត់បន្ថយការចង peptide ទៅនឹងអ្នកទទួលគោលដៅ។ប៉ុន្តែភាពស្និទ្ធស្នាលទាបរបស់ PEG peptides ជាធម្មតាត្រូវបានទូទាត់ដោយពាក់កណ្តាលជីវិតឱសថសាស្រ្តយូរជាងរបស់ពួកគេ ហើយដោយមានវត្តមាននៅក្នុងខ្លួនយូរជាងនេះ PEG peptides មានលទ្ធភាពកាន់តែច្រើនក្នុងការស្រូបចូលទៅក្នុងជាលិកាគោលដៅ។ដូច្នេះ លក្ខណៈបច្ចេកទេស PEG polymer គួរតែត្រូវបានធ្វើឱ្យប្រសើរសម្រាប់លទ្ធផលដ៏ល្អប្រសើរ។ម៉្យាងវិញទៀត PEG peptides កកកុញនៅក្នុងថ្លើមដោយសារតែការថយចុះនៃការបោសសំអាតតម្រងនោមដែលបណ្តាលឱ្យមានរោគសញ្ញា macromolecular ។ដូច្នេះ ការកែប្រែ PEG ចាំបាច់ត្រូវតែត្រូវបានរចនាឡើងយ៉ាងប្រុងប្រយ័ត្នបន្ថែមទៀត នៅពេលដែល peptides ត្រូវបានប្រើសម្រាប់ការធ្វើតេស្តថ្នាំ។
ក្រុមកែប្រែទូទៅនៃអ្នកកែប្រែ PEG អាចត្រូវបានសង្ខេបដូចតទៅ៖ អាមីណូ (-amine) -NH2, aminomethyl-Ch2-NH2, hydroxy-OH, carboxy-Cooh, sulfhydryl (-Thiol) -SH, Maleimide -MAL, succinimide carbonate - SC, succinimide acetate -SCM, succinimide propionate -SPA, n-hydroxysuccinimide -NHS, Acrylate-ch2ch2cooh, aldehyde -CHO (ដូចជា propional-ald, butyrALD), មូលដ្ឋាន acrylic (-acrylate-acrl), azido-azide, biotiny Biotin, Fluorescein, glutaryl -GA, Acrylate Hydrazide, alkyne-alkyne, p-toluenesulfonate -OTs, succinimide succinate -SS ជាដើម។ និស្សន្ទវត្ថុ PEG ដែលមានអាស៊ីត carboxylic អាចត្រូវបានផ្សំជាមួយ amines n-terminal ឬ lysine sides ។PEG ដែលត្រូវបានធ្វើឱ្យសកម្មអាមីណូអាចត្រូវបានផ្សំជាមួយខ្សែសង្វាក់ចំហៀងនៃអាស៊ីត aspartic ឬអាស៊ីត glutamic ។Mal-activated PEG អាចត្រូវបានភ្ជាប់ជាមួយ mercaptan នៃខ្សែសង្វាក់ចំហៀង cysteine ដែលត្រូវបានការពារយ៉ាងពេញលេញ [11] ។អ្នកកែប្រែ PEG ត្រូវបានចាត់ថ្នាក់ជាទូទៅដូចខាងក្រោម (ចំណាំ៖ mPEG គឺ methoxy-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) ការកែប្រែខ្សែសង្វាក់ត្រង់ PEG
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) កម្មវិធីកែប្រែ PEG ដែលមានមុខងារ
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) ការកែប្រែ PEG សាខា
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinization
Biotin អាចត្រូវបានចងយ៉ាងខ្លាំងជាមួយ avidin ឬ streptavidin ហើយភាពរឹងមាំនៃការចងគឺជិតនឹងចំណងកូវ៉ាលេន។សារធាតុ peptides ដែលមានស្លាក Biotin ត្រូវបានគេប្រើជាទូទៅនៅក្នុង immunoassay, histocytochemistry, និង fluorescence-flow cytometry ។អង់ទីករអង់ទីប៊ីយ៉ូទីនដែលមានស្លាកក៏អាចត្រូវបានប្រើដើម្បីចង peptides biotinylated ។ស្លាក Biotin ជារឿយៗត្រូវបានភ្ជាប់ទៅខ្សែសង្វាក់ចំហៀង lysine ឬស្ថានីយ N ។អាស៊ីត 6-aminocaproic ត្រូវបានគេប្រើជាញឹកញាប់ជាចំណងរវាង peptides និង biotin ។ចំណងគឺអាចបត់បែនបានក្នុងការចងទៅនឹងស្រទាប់ខាងក្រោម ហើយចងបានប្រសើរជាងមុននៅក្នុងវត្តមាននៃឧបសគ្គស្តេរីក។
9. ស្លាកសញ្ញា fluorescent
ការដាក់ស្លាក fluorescent អាចត្រូវបានប្រើដើម្បីតាមដាន polypeptides នៅក្នុងកោសិការស់ និងដើម្បីសិក្សាអំពីអង់ស៊ីម និងយន្តការនៃសកម្មភាព។Tryptophan (Trp) គឺ fluorescent ដូច្នេះវាអាចត្រូវបានប្រើសម្រាប់ការដាក់ស្លាកខាងក្នុង។វិសាលគមនៃការបំភាយសារធាតុ tryptophan អាស្រ័យលើបរិយាកាសជុំវិញ និងថយចុះជាមួយនឹងការថយចុះប៉ូលនៃសារធាតុរំលាយ ដែលជាទ្រព្យសម្បត្តិដែលមានប្រយោជន៍សម្រាប់ការរកឃើញរចនាសម្ព័ន្ធ peptide និងការចងអ្នកទទួល។Tryptophan fluorescence អាចត្រូវបានពន្លត់ដោយអាស៊ីត aspartic protonated និងអាស៊ីត glutamic ដែលអាចកំណត់ការប្រើប្រាស់របស់វា។ក្រុម Dansyl chloride (Dansyl) មាន fluorescent ខ្ពស់នៅពេលភ្ជាប់ទៅនឹងក្រុមអាមីណូ ហើយជារឿយៗត្រូវបានគេប្រើជាស្លាក fluorescent សម្រាប់អាស៊ីតអាមីណូ ឬប្រូតេអ៊ីន។
ការបំប្លែងថាមពលពន្លឺ (FRET) មានប្រយោជន៍សម្រាប់ការសិក្សាអង់ស៊ីម។នៅពេលដែល FRET ត្រូវបានអនុវត្ត សារធាតុ polypeptide ស្រទាប់ខាងក្រោមជាធម្មតាមានក្រុម fluorescence-labeling និងក្រុម fluorescence-quenching ។ក្រុម fluorescent ដែលមានស្លាកត្រូវបានពន្លត់ដោយ quencher តាមរយៈការផ្ទេរថាមពលដែលមិនមែនជារូបថត។នៅពេលដែល peptide ត្រូវបានផ្តាច់ចេញពីអង់ស៊ីមនៅក្នុងសំណួរ ក្រុមដាក់ស្លាកបញ្ចេញ fluorescence ។
10. ទ្រុង polypeptides
Cage peptides មានក្រុមការពារដែលអាចដកចេញបានដោយអុបទិក ដែលការពារ peptide ពីការចងទៅនឹងអ្នកទទួល។នៅពេលដែលប៉ះពាល់នឹងកាំរស្មី UV សារធាតុ peptide ត្រូវបានធ្វើឱ្យសកម្ម ស្តារភាពស្និទ្ធស្នាលរបស់វាទៅនឹងអ្នកទទួល។ដោយសារការធ្វើឱ្យសកម្មអុបទិកនេះអាចត្រូវបានគ្រប់គ្រងដោយយោងទៅតាមពេលវេលា ទំហំ ឬទីតាំងនោះ peptides ទ្រុងអាចត្រូវបានប្រើដើម្បីសិក្សាពីប្រតិកម្មដែលកើតឡើងនៅក្នុងកោសិកា។ក្រុមការពារដែលប្រើជាទូទៅបំផុតសម្រាប់ polypeptides ទ្រុងគឺក្រុម 2-nitrobenzyl និងដេរីវេនៃពួកវា ដែលអាចត្រូវបានណែនាំនៅក្នុងការសំយោគ peptide តាមរយៈដេរីវេនៃអាស៊ីតអាមីណូការពារ។ដេរីវេនៃអាស៊ីតអាមីណូដែលត្រូវបានបង្កើតឡើងគឺ lysine, cysteine, serine និង tyrosine ។ទោះជាយ៉ាងណាក៏ដោយ ដេរីវេនៃ Aspartate និង glutamate មិនត្រូវបានគេប្រើជាទូទៅទេ ដោយសារតែភាពងាយនឹងកើតមានរបស់ពួកគេចំពោះវដ្ត កំឡុងពេលសំយោគ peptide និង dissociation ។
11. Polyantigenic peptide (MAP)
ជាធម្មតា peptides ខ្លីគឺមិនមានភាពស៊ាំទេ ហើយត្រូវតែត្រូវបានភ្ជាប់ជាមួយប្រូតេអ៊ីនដឹកជញ្ជូនដើម្បីបង្កើតអង្គបដិប្រាណ។Polyantigenic peptide (MAP) ត្រូវបានផ្សំឡើងពី peptides ដូចគ្នាបេះបិទជាច្រើនដែលតភ្ជាប់ទៅ nuclei lysine ដែលអាចបង្ហាញនូវសារធាតុ immunogens ដ៏មានថាមពលខ្ពស់ និងអាចប្រើដើម្បីរៀបចំប្រូតេអ៊ីន peptide-carrier ។MAP polypeptides អាចត្រូវបានសំយោគដោយការសំយោគដំណាក់កាលរឹងនៅលើជ័រ MAP ។ទោះជាយ៉ាងណាក៏ដោយ ការភ្ជាប់គ្នាមិនពេញលេញនាំឱ្យខ្សែសង្វាក់ peptide បាត់ ឬកាត់បន្ថយនៅលើសាខាមួយចំនួន ហើយដូច្នេះមិនបង្ហាញលក្ខណៈសម្បត្តិនៃ MAP polypeptide ដើមនោះទេ។ជាជម្រើសមួយ peptides អាចត្រូវបានរៀបចំ និងបន្សុតដោយឡែកពីគ្នា ហើយបន្ទាប់មកភ្ជាប់ជាមួយ MAP ។លំដាប់ peptide ដែលភ្ជាប់ទៅនឹងស្នូល peptide ត្រូវបានកំណត់យ៉ាងល្អ និងងាយស្រួលកំណត់ដោយម៉ាស់។
សេចក្តីសន្និដ្ឋាន
ការកែប្រែ Peptide គឺជាមធ្យោបាយសំខាន់នៃការរចនា peptides ។peptides ដែលត្រូវបានកែប្រែដោយគីមីមិនត្រឹមតែអាចរក្សាបាននូវសកម្មភាពជីវសាស្រ្តខ្ពស់ប៉ុណ្ណោះទេ ប៉ុន្តែថែមទាំងអាចជៀសវាងនូវគុណវិបត្តិនៃភាពស៊ាំ និងការពុលយ៉ាងមានប្រសិទ្ធភាពផងដែរ។ក្នុងពេលជាមួយគ្នានេះ ការកែប្រែគីមីអាចផ្តល់ឱ្យ peptides ជាមួយនឹងលក្ខណៈសម្បត្តិល្អថ្មីមួយចំនួន។ក្នុងប៉ុន្មានឆ្នាំថ្មីៗនេះវិធីសាស្រ្តនៃការធ្វើឱ្យសកម្ម CH សម្រាប់ការកែប្រែក្រោយការកែប្រែនៃសារធាតុ polypeptides ត្រូវបានបង្កើតឡើងយ៉ាងឆាប់រហ័ស ហើយលទ្ធផលសំខាន់ៗជាច្រើនត្រូវបានសម្រេច។
ពេលវេលាប្រកាស៖ ថ្ងៃទី ២០-២៣ ខែមីនា
